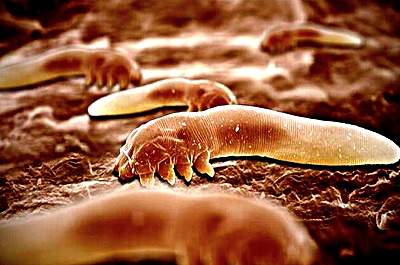
Многие глисты проходят в своем развитии несколько этапов:
- яйцо,
- личинка,
- зрелая особь.
Они могут иметь специфические зоны проникновения, пути миграции и места обитания. Поэтому и реакция организма на присутствующих в нем паразитов может существенно варьировать не только в зависимости от вида гельминтов, но и от стадии их развития и времени, прошедшего с момента заражения. Противоглистный иммунитет — защита организма от глистов — является комплексным. В нем участвуют:
- клетки врожденного и приобретенного иммунитета,
- клетки неиммунной природы,
- цитокины,
- антитела,
- комплемент.
Однако, несмотря на своеобразие включаемых при конкретных нозологических формах защитных механизмов, общим проявлением противоглистного иммунитета, определяющим устойчивость к инвазии глистов, считается индукция дифференцировки лимфоцитов по Th2-пути.
Действительно, многие экспериментальные исследования демонстрируют, что попытки блокирования Th2-отклонения (например, через генетический нокаут IL-4) или усиление Th1-реактивности сопровождается ослаблением антигельминтного иммунитета. Второй принципиальный момент состоит в том, что высокая противоглистная активность иммунной системы проявляется, главным образом, на ранних этапах паразитарной инвазии. В том случае, если такая реактивность не увенчалась эффективной девастацией глистов, наступает ее постепенное подавление. Включение механизмов иммуносупрессии в основном направлено на сбережение макроорганизма. При этом необходимо отметить, что вновь формируемые отношения «паразит-хозяин» скорее имеют симбиотический, нежели антагонистический характер.
Механизм противоглистного иммунитета
- деструктивного воздействия на паразита,
- механического изгнания глистов.
Разрушение паразита
Наибольшей разрушительной способностью среди эффекторных клеток противоглистного иммунитета обладают эозинофилы. Эпидемиологические исследования свидетельствуют о прямой корреляции между эозинофилией и резистентностью к глистной инфекции. In vivo скопления эозинофилов отмечаются в непосредственной близости от паразитов, a in vitro в присутствии антител и комплемента эти клетки дегранулируют и способны убивать чужеродные организмы. Однако их эффективность наиболее четко проявляется при воздействии на личинки и в значительно меньшей степени — на половозрелые особи.
Изгнание глистов
Изгнание глистов происходит преимущественно через желудочно-кишечный тракт, где они чаще всего откладывают яйца. Важную роль в этом процессе играют тучные клетки. Приток мастоцитов, как правило, обусловлен Th2-цитокинами (IL-4, IL-9, II-13), а также SCF (с-kit-лиганд). Прибывающие и делящиеся in situ тучные клетки активно связывают на своей поверхности IgE, направленные против антигенов гельминтов. Эти антитела образуются место В-лимфоцитами под влиянием IL-4 и IL-13, синтезируемых Th2-лимфоцитами. Связывание гельминтных антигенов с IgE приводит к дегрануляции тучных клеток, что сопровождается целым спектром эффектов. Высвобождение гистамина инициирует секрецию электролитов и движение воды (пассивно) в полость кишечника. Под влиянием лейкотриенов и простагландинов приток воды в кишку еще больше усиливается, активируется ее гладкая мускулатура. Кроме того, лейкотриены стимулируют секрецию муцинов бокаловидными клетками. Эти содержащие сульфаты гликопротеины (как и протеогликаны мастоцитов) обладают парализующим действием на глистов. Результатом этого комплексного процесса является конечная цель противоглистного иммунитета — быстрое опорожнение кишечника с изгнанием паразитов.
К.В. Шмагель и В.А. Черешнев